发表期刊:ACS Nano
IF:17.1
一作单位:中国科学院长春应用化学研究所
研究背景
缺血性中风是一种具有高死亡率和致残风险的神经功能障碍,缺氧或缺血会导致线粒体功能障碍,引发一系列恶性事件,包括氧化损伤、小胶质细胞激活、炎症过程和神经元死亡等。由氧化应激和炎症因子主要引发的血脑屏障(BBB) 损伤伴随细胞旁通透性增加,会导致不受调控的血脑交换,加剧中风。缺血性中风导致BBB开放后,药物得以不受控地进入大脑,这为给药提供了契机,但同时也与试图封闭BBB的保护性治疗策略形成了矛盾。跨细胞途径是穿透BBB并将治疗药物选择性递送至大脑的可行替代方案。多酚类物质通过诱导保护性自噬、修复BBB损伤、抑制小胶质细胞极化、炎症因子、凋亡相关蛋白及氧化应激损伤等多重途径,已成为缺血性中风的治疗方案。同时,多酚复合物含有的儿茶酚和邻苯三酚活性基团,能通过多种相互作用与其他物质结合,为构建多功能递送系统提供了有利条件。
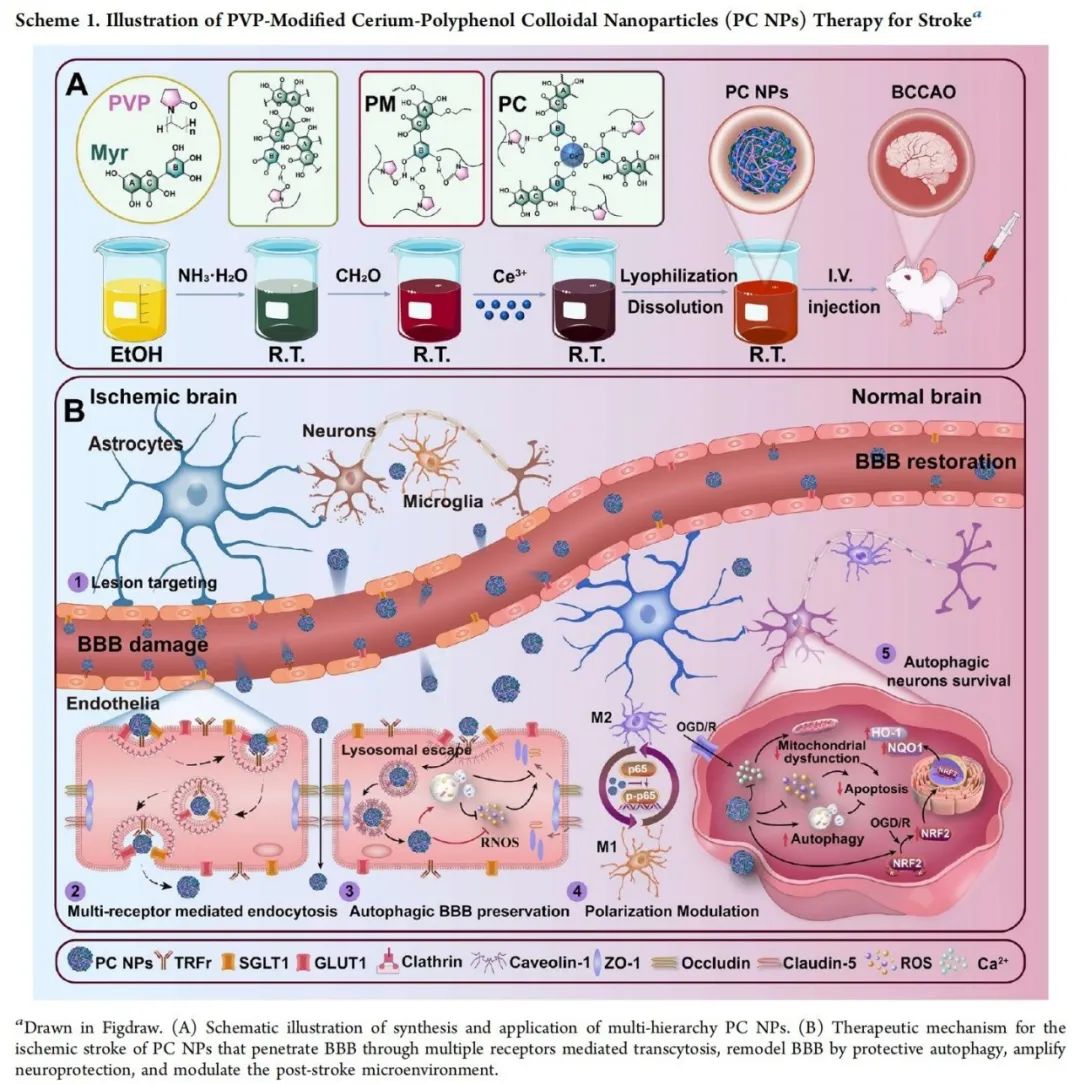
本研究开发了一种针对缺血性中风的多层次治疗策略:通过多重受体介导的胞吞作用穿透BBB,并利用保护性自噬对其进行重塑,同时调控中风后微环境。研究开发了一种掺杂Ce的杨梅素(Myr) 低聚物衍生的纳米结构,该结构能够通过由葡萄糖转运体和铁转运体共同介导的BBB,并通过激活保护性自噬来调节紧密连接蛋白(TJs) 的表达,从而展现出修复BBB的能力。Myr低聚物骨架不仅作为靶向部分,更是继承了Myr所有多样化药理活性的显著活性实体。其对氧化损伤、M1小胶质细胞活化及炎症因子的抑制,使这一单组分纳米剂兼具骨架结构、靶向域和治疗成分的多重功能。
 实验结果
实验结果
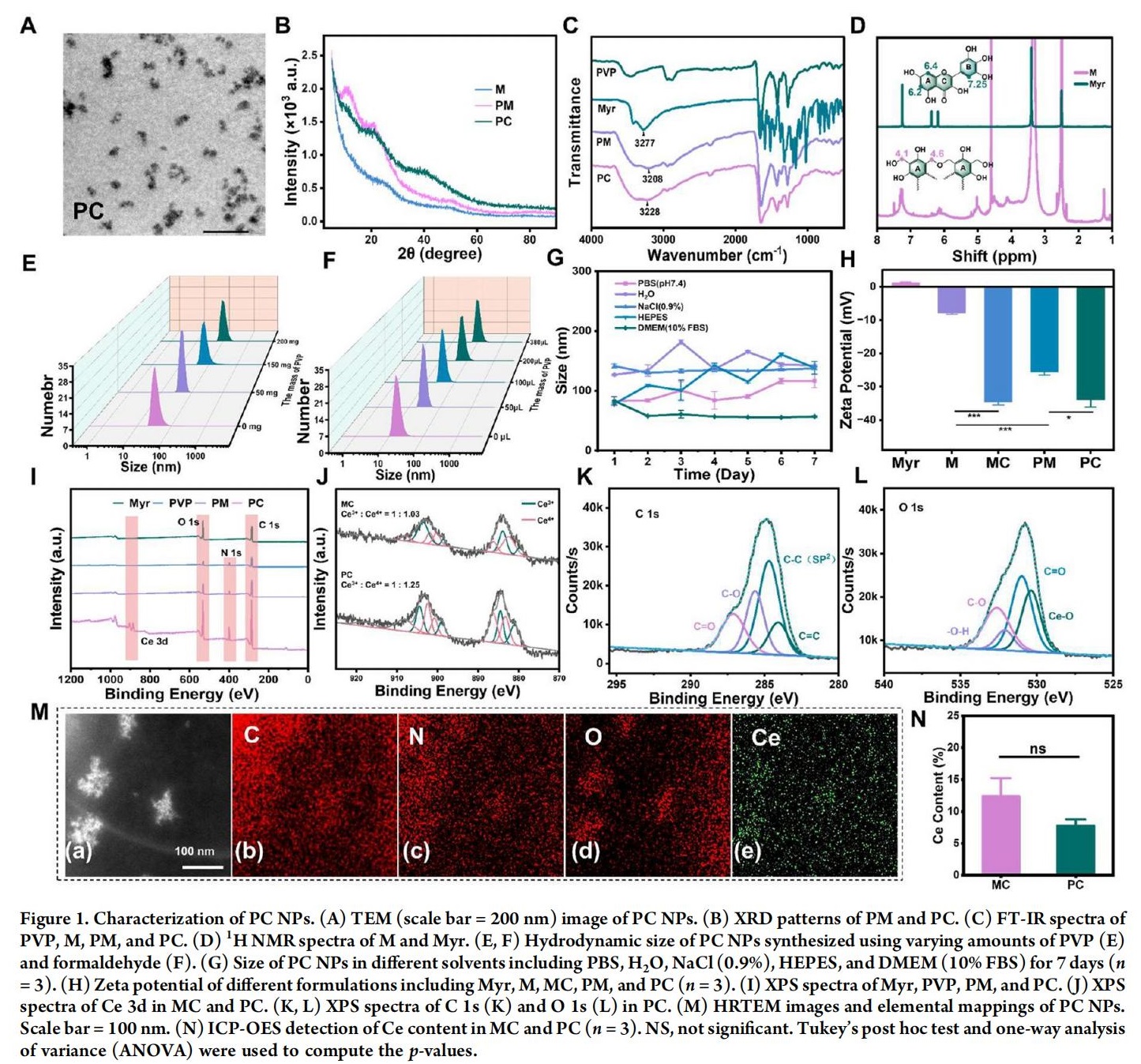
1.PC NPs的合成与表征
采用溶胶-凝胶技术和组装工艺制备了聚乙烯吡咯烷酮(PVP) 修饰的Ce-多酚胶体纳米颗粒(PC NPs)。首先选择具有神经保护作用的多酚类化合物Myr作为骨架成分,通过拜耳反应合成Myr低聚物,再与PVP共组装形成针状纳米结构(PM NPs),通过螯合组装将Ce离子掺杂到PM中,获得具有松散结构且高稳定性的胶体纳米颗粒(PC NPs)。
2.ROS清除特性
活性氧(ROS) 和活性氮(RNS) (统称RNOS) 的生成与清除失衡可能导致氧化应激和过度炎症反应,加剧缺血性损伤。与不含Ce的PM NPs相比,PC NPs具有ROS/RNS清除能力,展现了其潜在的多酶模拟特性,更强的总抗氧化能力(T-AOC) 也证明其具有突出的缺血再灌注(I/R) 疾病治疗应用潜力。PC NPs对细胞内ROS的清除效果同样优异,在抵抗H₂O₂诱导的ROS应激时,具有最佳维持正常细胞线粒体膜电位(MMP) 的能力,通过降低细胞内ROS水平,显著缓解线粒体功能障碍和细胞凋亡,保护细胞免受氧化损伤。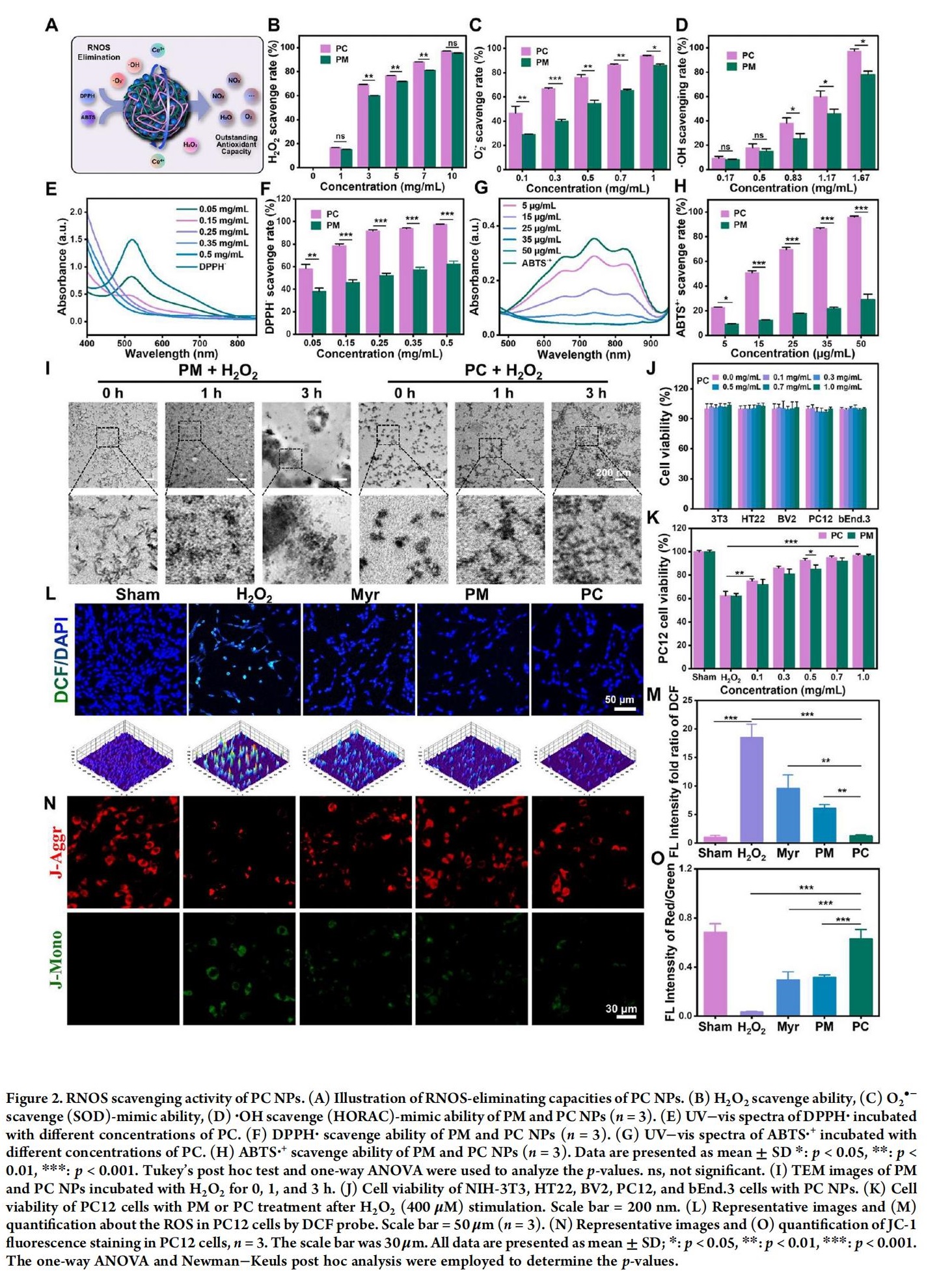 3.抗氧糖剥夺/再灌注(OGD/R) 诱导缺血级联反应的抗凋亡作用
3.抗氧糖剥夺/再灌注(OGD/R) 诱导缺血级联反应的抗凋亡作用
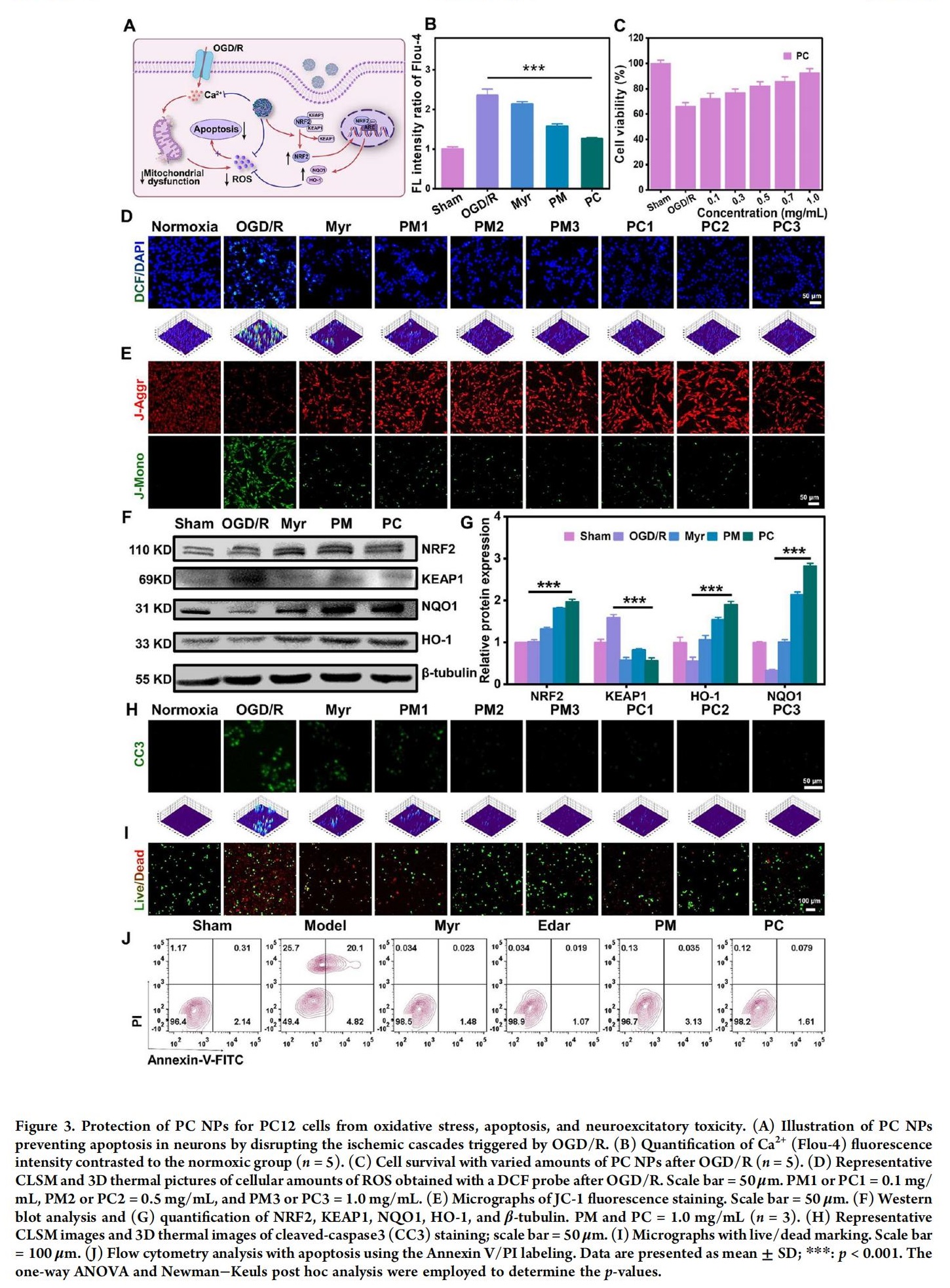
I/R可触发缺血级联反应,包括兴奋性毒性和神经细胞氧化损伤。在缺血状态下,能量耗竭和离子泵功能障碍导致细胞内钙离子过量,通过释放谷氨酸激活神经元兴奋性中毒,引发早期缺血性细胞死亡。PC NPs能有效保护细胞免受OGD/R后由兴奋性毒性和氧化应激等缺血性损伤引发的细胞凋亡。通过降低细胞内钙离子含量,发挥神经保护作用。增加NRF2及其下游氧化蛋白表达来激活NRF2/HO-1通路,减少ROS产生,抑制氧化应激反应并促进氧化还原平衡。同时也能显著降低被激活的cleaved-caspase 3(CC3)蛋白水平,保护细胞免受OGD/R诱导的细胞凋亡,提升细胞存活率。
4.自噬激活与BBB体外保护
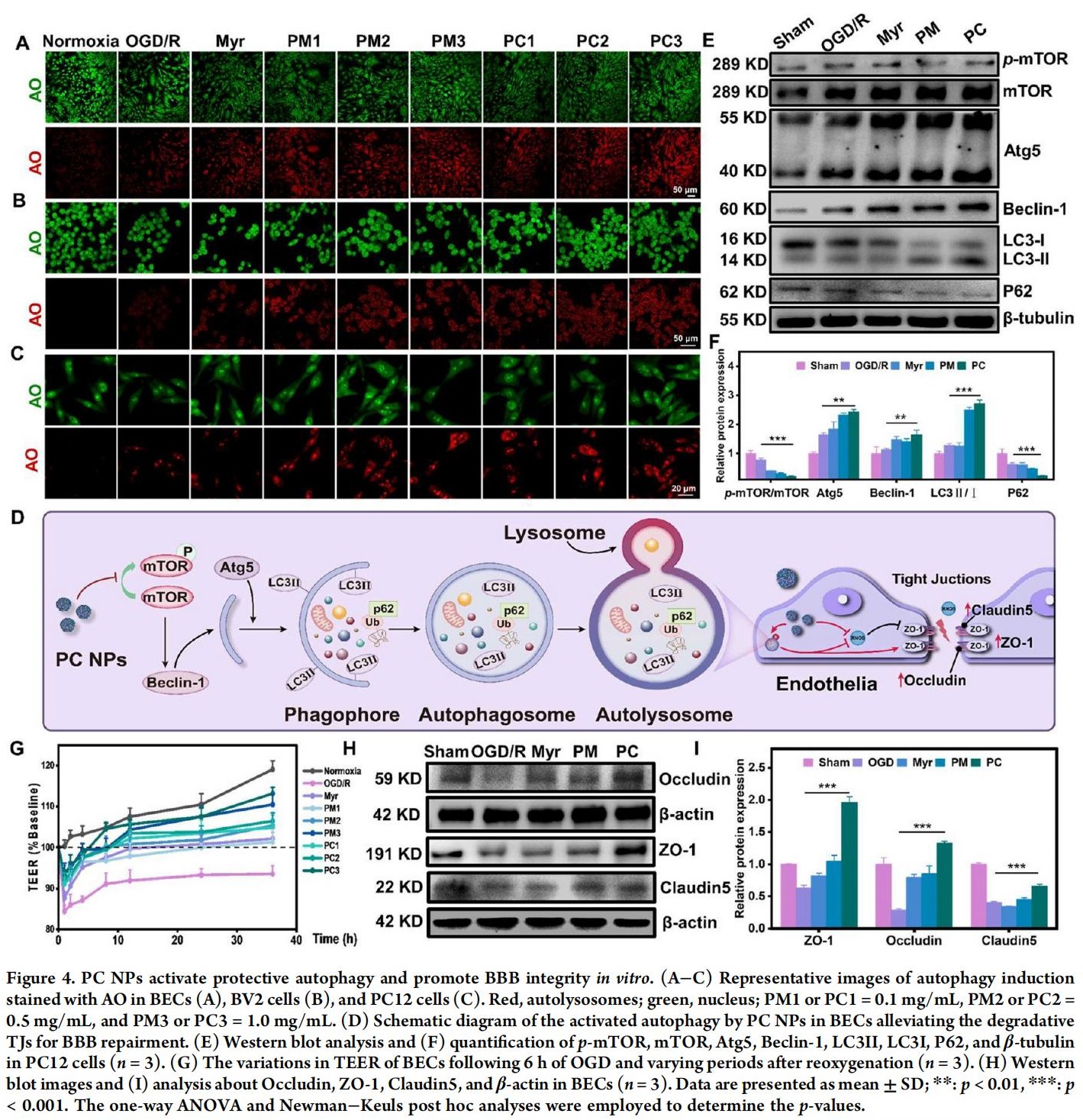
在缺氧/低糖条件下,缺血性中风期间不仅神经元需要高度激活自噬来抑制异常细胞器和蛋白质的积累,神经胶质细胞同样如此。适度诱导自噬可防止细胞发生一系列缺血级联反应。
Myr具有上调自噬的能力,而Ce掺杂进一步增强了PC NPs的自噬调控能力,这可能与其更强的抗氧化能力和更快的内吞作用相关。氧糖剥夺/复氧处理后细胞单层及BBB完整性受损,而PC NPs显示出脑血管修复能力,这表明PC NPs可通过抑制mTOR通路激活自噬对抗I/R损伤,从而逆转BBB降解,修复受损屏障并增强神经元存活能力。
 5.BBB穿透与内吞机制
5.BBB穿透与内吞机制
缺血性中风后,能量耗竭会激活一系列调节过程以适应多重代谢紊乱,导致多种细胞质膜锚定转运体和受体上调表达。缺血性中风后被脑内皮细胞(BCEs) 过度表达的代表性受体有葡萄糖转运蛋白1(GLU1)、钠-葡萄糖协同转运蛋白(SGLT) 和转铁蛋白受体(TfR),这些受体能够帮助细胞适应缺血/低血糖状态下葡萄糖和铁的异常摄取。
PC NPs可与缺氧/低血糖条件下BECs中过表达的GLUT1、SGLT1等转运蛋白相互作用,促进其内吞作用从而实现BBB穿透。BECs对PC NPs的内化涉及多条通路:网格蛋白和SGLT1在内吞过程中起主导作用,小窝蛋白、TfR和GLUT1也承担重要内化功能。多酚类物质可通过GLUT1和SGLT1等葡萄糖转运体被细胞摄取,部分镧系元素则依赖TfR内化。显然PC NPs同时继承了Myr和Ce的多重特性,具备多受体介导的双重内吞途径,以及小窝/网格蛋白依赖的内化机制,这种多元化的内化路径为其生物学效应提供了结构基础。

6.体外抗炎效应研究
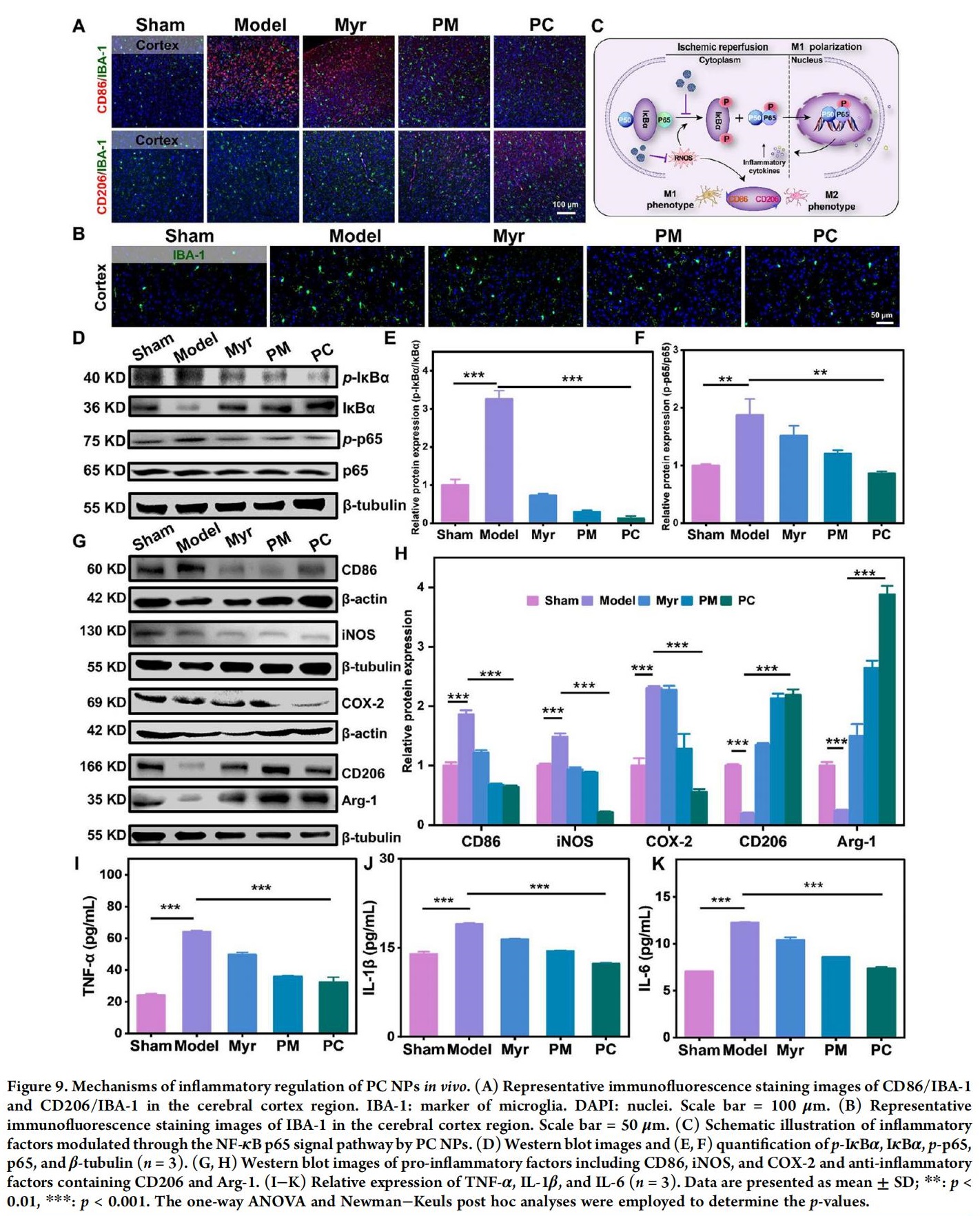
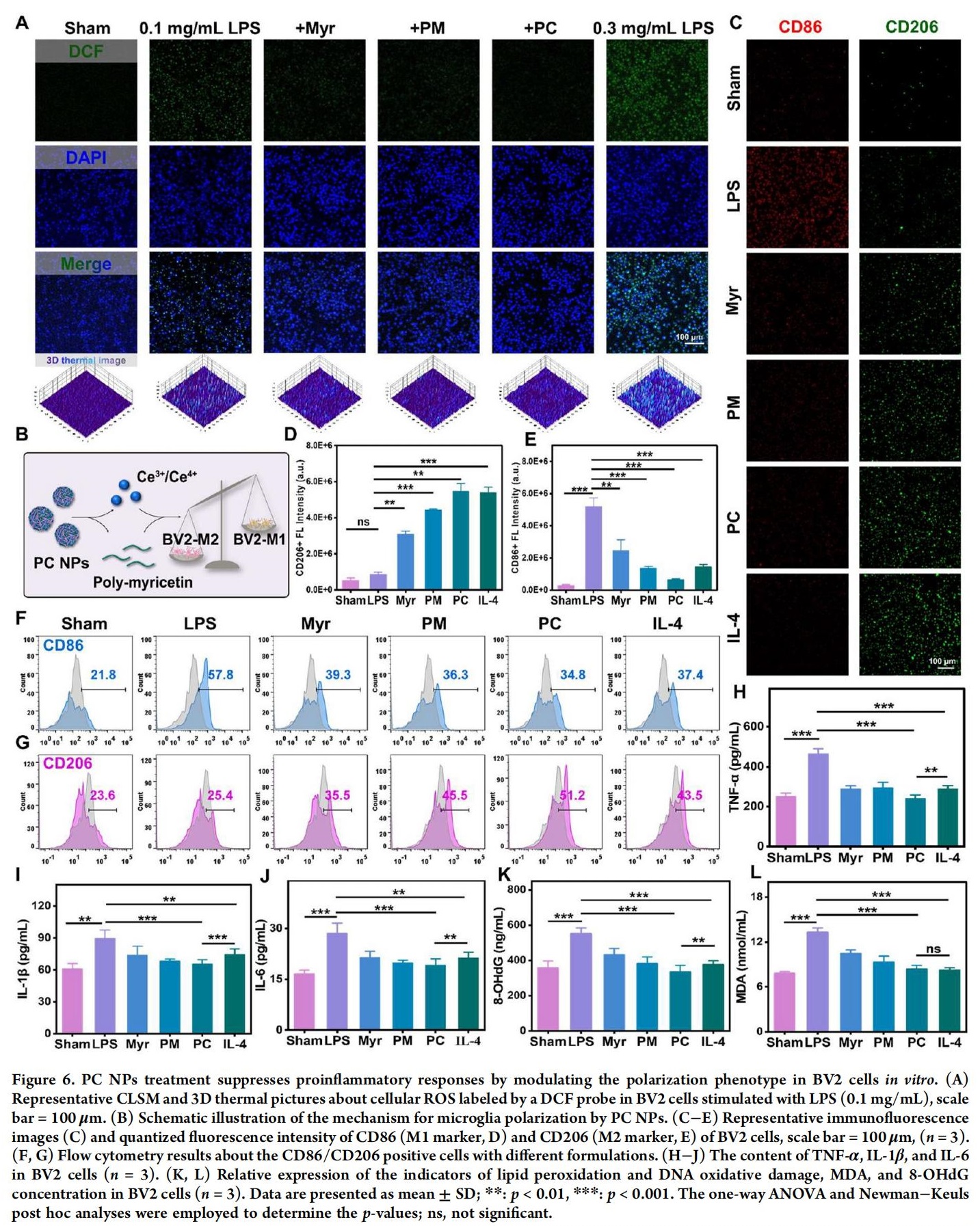
小胶质细胞通过减少神经元死亡、促进神经再生及加速神经功能恢复,在缺血性中风后发挥重要作用。该细胞具有两种表型:经典激活型(M1促炎表型) 和替代激活型(M2抗炎表型)。二者对脑功能恢复具有相反作用,前者通过产生有害的促炎细胞因子加剧脑损伤,而后者可减轻局部神经炎症并促进脑功能恢复。因此在脑I/R的治疗过程中,调控小胶质细胞向M2表型极化至关重要,通过促进抗炎M2表型极化,小胶质细胞可能恢复其他细胞的功能。PC NPs能显著促进小胶质细胞向M2型极化,以此进一步缓解I/R导致的脑炎症损伤。
7.脑I/R体内治疗效果研究
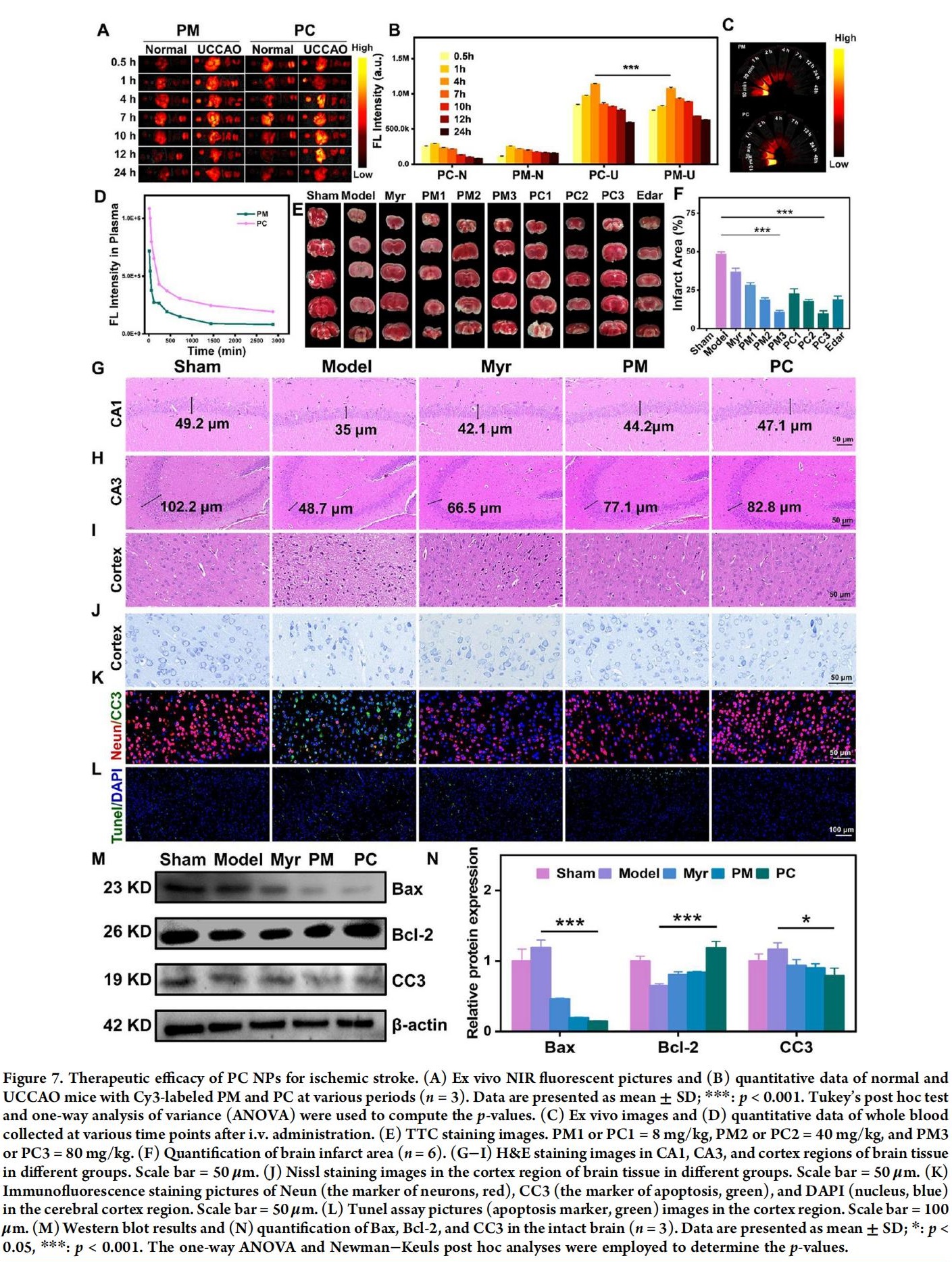
PC NPs能在中风后高效富集于脑部,Ce掺杂赋予了PC NPs更强的脑组织穿透优势。Ce掺杂不仅通过三价与四价态间的价态转换增强PC NPs的抗氧化能力,还与TfR依赖的内吞作用相关。
中风后被动性BBB渗漏与主动性跨细胞转运的叠加效应进一步提升了纳米制剂的脑部灌注量。PC NPs对神经元结构具有保护作用,能够减轻神经损伤,有效逆转神经元死亡,缩小脑梗死面积。此外,PC NPs还可以上调Bcl-2表达并抑制CC3和Bax,有效缓解I/R引发的细胞凋亡。
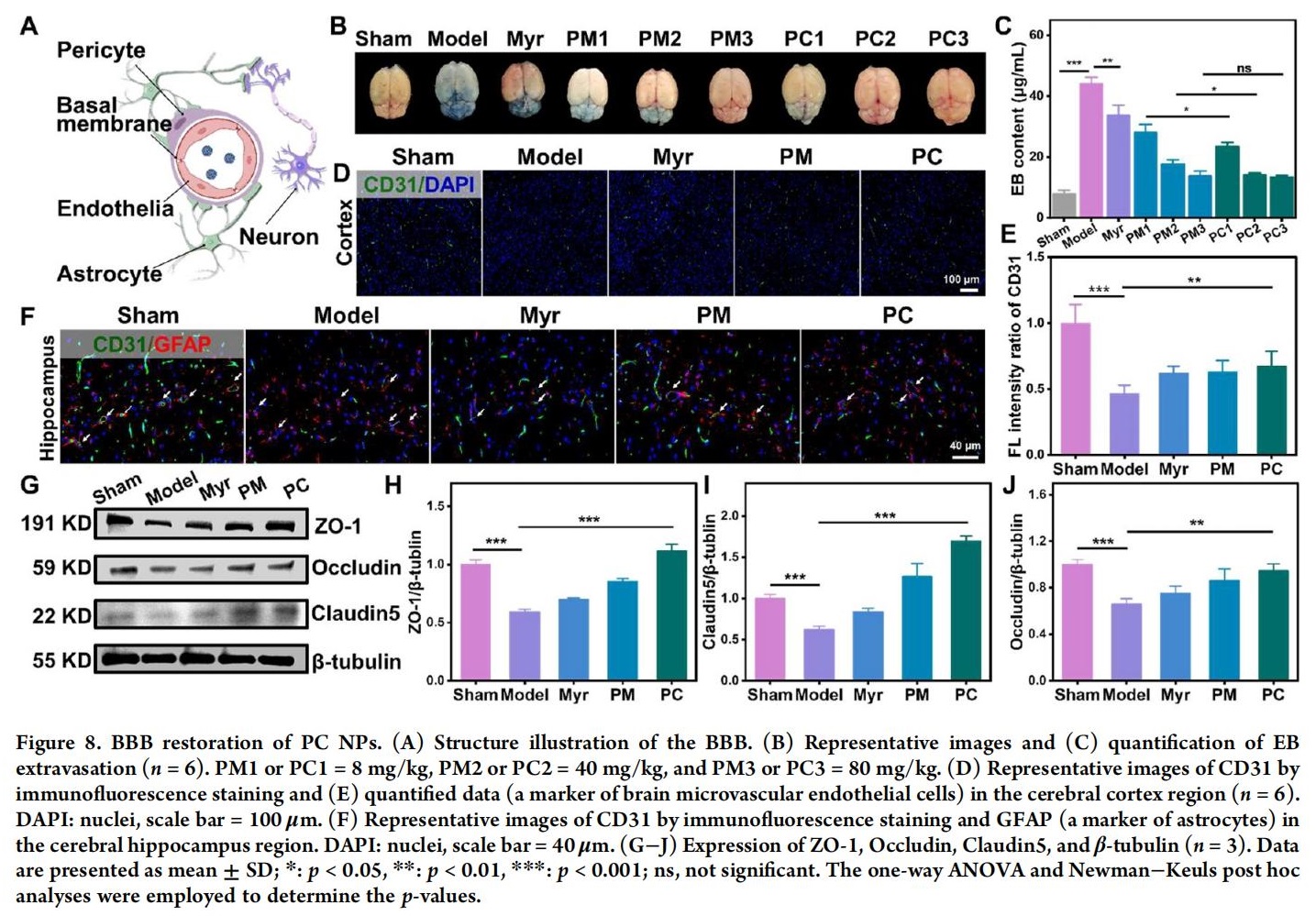
8.改善I/R造成的BBB损伤
BBB作为大脑的保护性屏障,能阻止有害生物和物质侵入。I/R后BBB的完整性和功能会遭到破坏,从而加剧缺血性中风的病理进程并改变其转归。PC NPs通过抑制TJs降解,有效减轻BBB破坏,保护血管形态完整性。
9.小胶质细胞极化调控逆转促炎微环境
I/R后,具有高吞噬活性的小胶质细胞被激活,极化为经典的促炎M1表型和抗炎M2表型。PC NPs可调节小胶质细胞极化,随着浓度升高,PC NPs诱导小胶质细胞向M2型极化的能力逐渐增强。此外,PC NPs能够抑制NF-κB通路,从而逆转I/R后的促炎微环境。